گلیکوژن در واقع نوعی از گلوکز است که در بدن ما ذخیره میشود.به عبارتی این ترکیب، ساختاری پلی ساکاریدی از گلوکز می باشد.در این بخش از قرار است بیشتر با این گلوکز و ساختار آن آشنا شوید.
گلیکوژن چیست ؟
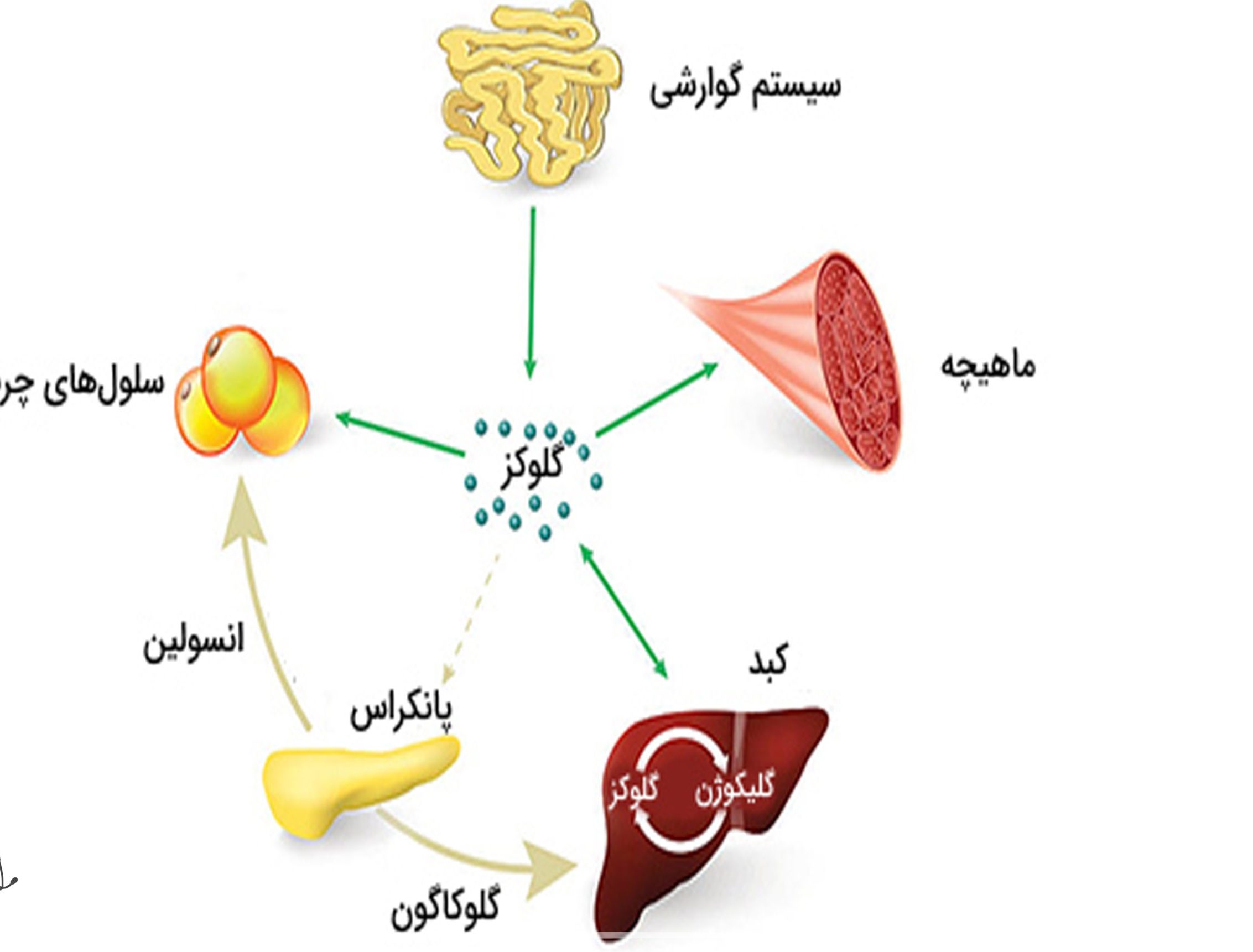
گلیکوژن شکل ذخیرهشده گلوکز است که از تعداد زیادی مولکولهای متصلشده گلوکز تشکیل میشود. گلوکز (قند) منبع اصلی انرژی بدن است که از کربوهیدراتهای موجود در غذاها و نوشیدنیها دریافت میشود. وقتی انرژی بدن تأمین است و بدن موقتا به گلوکز غذایی که خوردهاید نیازی ندارد، گلوکز را در عضلات و کبد ذخیره میکند تا در مواقع لزوم از آن استفاده کند. این گلوکز ذخیرهشده در عضلات و کبد گلیکوژن نام دارد.
بدن گیلیکوژن را از طریق فرایندی بهنام گلیکوژنز تولید میکند و در مواقع لزوم از طریق فرایندی بهنام گلیکوژنولیز آن را تجزیه و برای استفاده آماده میکند. چندین آنزیم مختلف مسئول این دو فرایند و سنتز گلیکوژن هستند. آنزیم نوعی پروتئین در سلول است که نقش کاتالیزور را دارد. در بدن ما هزاران آنزیم وجود دارند که هرکدام مسئولیت منحصربهفردی دارند.
تفاوت ساختار با گلوکز و گلوکاگون
گرچه گیلیکوژن و گلوکز و گلوکاگون همگی به استفاده بدن از غذاهای پرکربوهیدرات مربوطاند، هرکدام عملکرد متفاوتی دارند. گلوکز از کربوهیدراتهای موجود در غذاهایی که میخورید، تأمین میشود. گلوکز خون (قند خون) قند اصلی موجود در خون است. این قند منبع مهم انرژی است و مواد مغذی را برای اندامها، ماهیچهها و سیستم عصبی بدن فراهم میکند. گلوکز برای بدن بسیار مهم است، چون منبع اصلی انرژی موردنیاز مغز محسوب میشود. در واقع نیاز ثابت مغز به گلوکز دلیل اصلی اهمیت تأمین گلوکز کافی در طول روز است. مقدار کربوهیدرات توصیهشده برای بزرگسالان حداقل ۱۳۰ گرم در روز است.
وقتی بدن نیاز فوری به گلوکز نداشته باشد، آن را بهشکل گیلیکوژن در کبد و عضلات ذخیره میکند. گلوکاگون هورمونی است که لوزالمعده میسازد و باعث میشود گلیکوژن دوباره به گلوکز تبدیل شود. این گلوکز وارد جریان خون میشود و بدن میتواند از آن برای تأمین انرژی استفاده کند. گلوکاگون و انسولین هورمونهای طبیعی و مهمیاند که میزان قند خون بدن را تنظیم میکنند.
همچنین در بخوانید : فواید کربوهیدرات پیچیده برای بدن چیست ؟
کجا ذخیره میشود ؟
بدن بیشترِ گلیکوژن را در کبد و ماهیچههای اسکلتی (ماهیچههای متصل به استخوانها و تاندونها) و مقادیر کمی از آن را در مغز ذخیره میکند. گرچه کبد بیشتر از ماهیچههای اسکلتی گلیکوژن ذخیره میکند، چون توده عضلانی بدن بیشتر از کبد است، حدود سهچهارم کل گلیکوژن بدن در ماهیچهها قرار دارد.
هنگام ورزش شدید و طولانیمدت، گلیکوژن موجود در سلولهای عضلانی فعال به میزان چشمگیری کاهش مییابد. مقدار گلیکوژن ذخیرهشده در سلولهای کبد به عوامل مختلفی بستگی دارد از جمله:
- مقدار کربوهیدرات مصرفی؛
- شدت و مدت فعالیتهای بدنی؛
- فاصله زمانی بین وعدههای غذایی.
پس از ۱۲ تا ۲۴ ساعت ناشتایی، تقریبا کل گلیکوژن کبد مصرف میشود.
در قارچ ها و باکتری ها
میکروارگانیسمها، مکانیسمهایی برای ذخیره انرژی و مقابله با محدودیت منابع غذایی در محیط خود دارند که ذخیره گلیکوژن یکی از این روشها است. محدودیت مواد مغذی (مقادیر کم کربن، فسفر، نیتروژن یا گوگرد) میتواند باعث ایجاد گلیکوژن در مخمر شود، در حالی که باکتریها، در پاسخ به منابع انرژی کربن موجود و محدودیت سایر مواد مغذی، گلیکوژن را سنتز میکنند. رشد باکتری و اسپور مخمر نیز با تجمع گلیکوژن در ارتباط هستند.

تاریخچه کشف
گلیکوژن، توسط «کلود برنارد» کشف شد. آزمایشهای او نشان داد که کبد مادهای دارد که میتواند با عمل تخمیر در کبد باعث احیای قند شود. در سال 1857، وی جداسازی مادهای را که «ماده قندساز» نامید را به انجام رساند. بلافاصله پس از کشف گلیکوژن در کبد، «A. Sanson» دریافت که بافت عضلانی نیز دارای ذخایر گلیکوژن است. فرمول تجربی این مولکول، توسط «Kekulé» در سال 1858 تعیین شد.
ساختار گلیکوژن چگونه است ؟
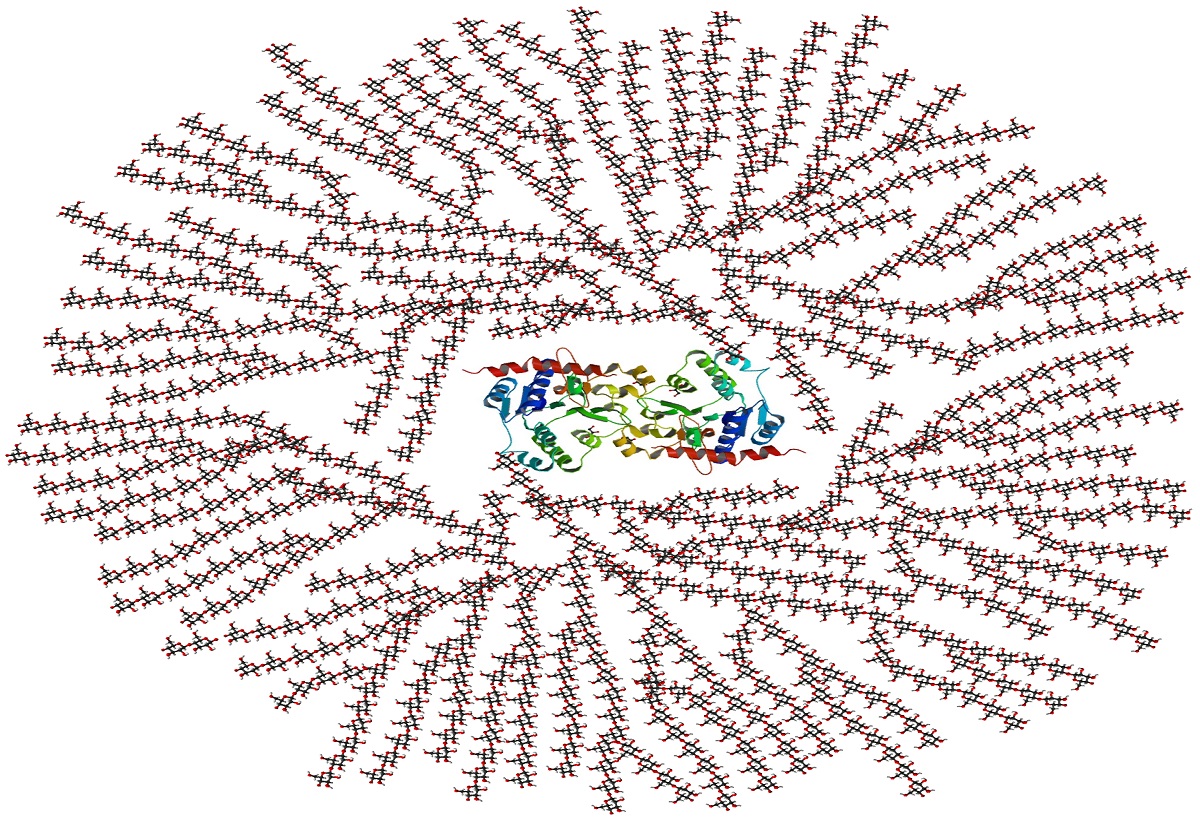
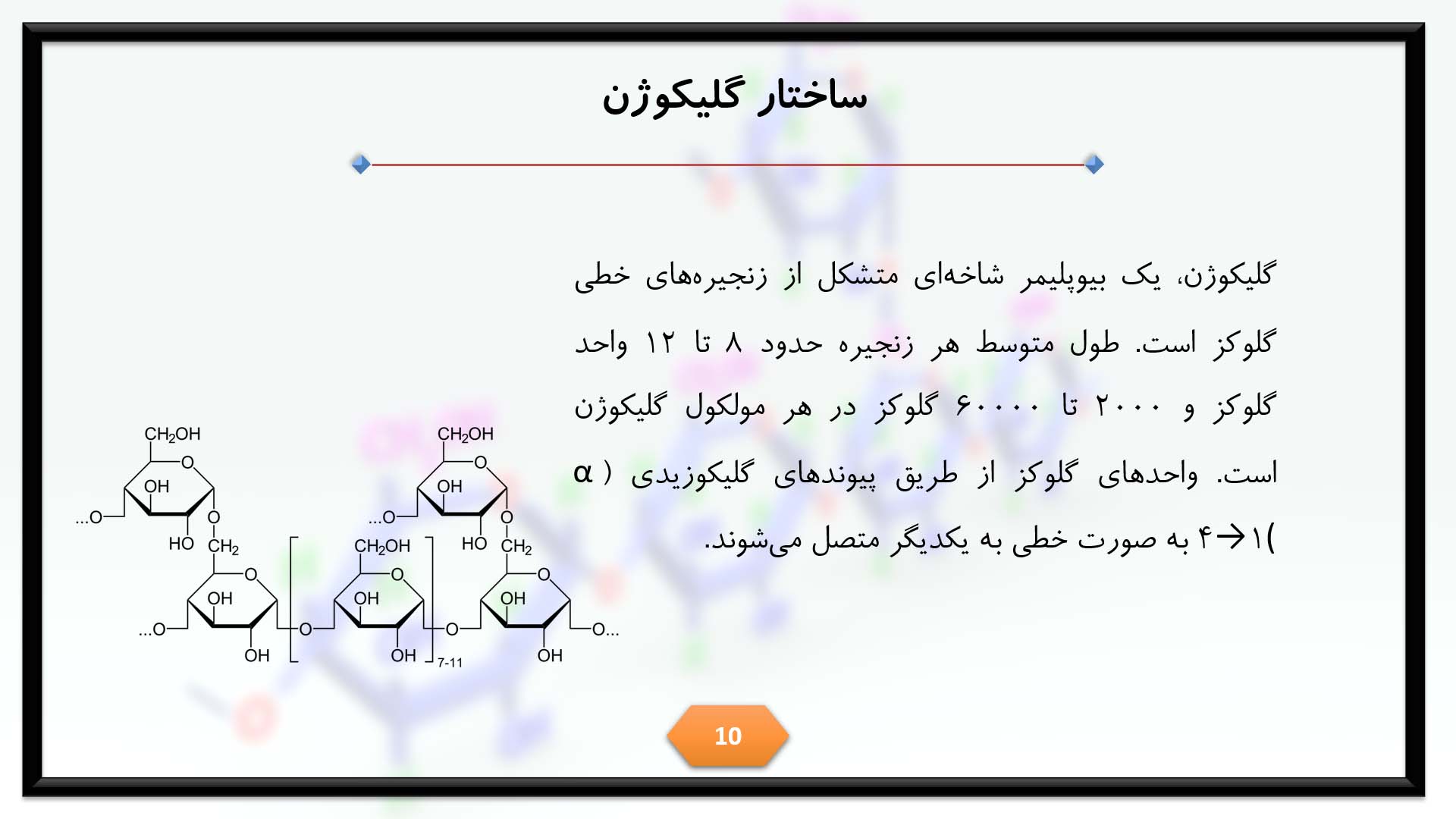
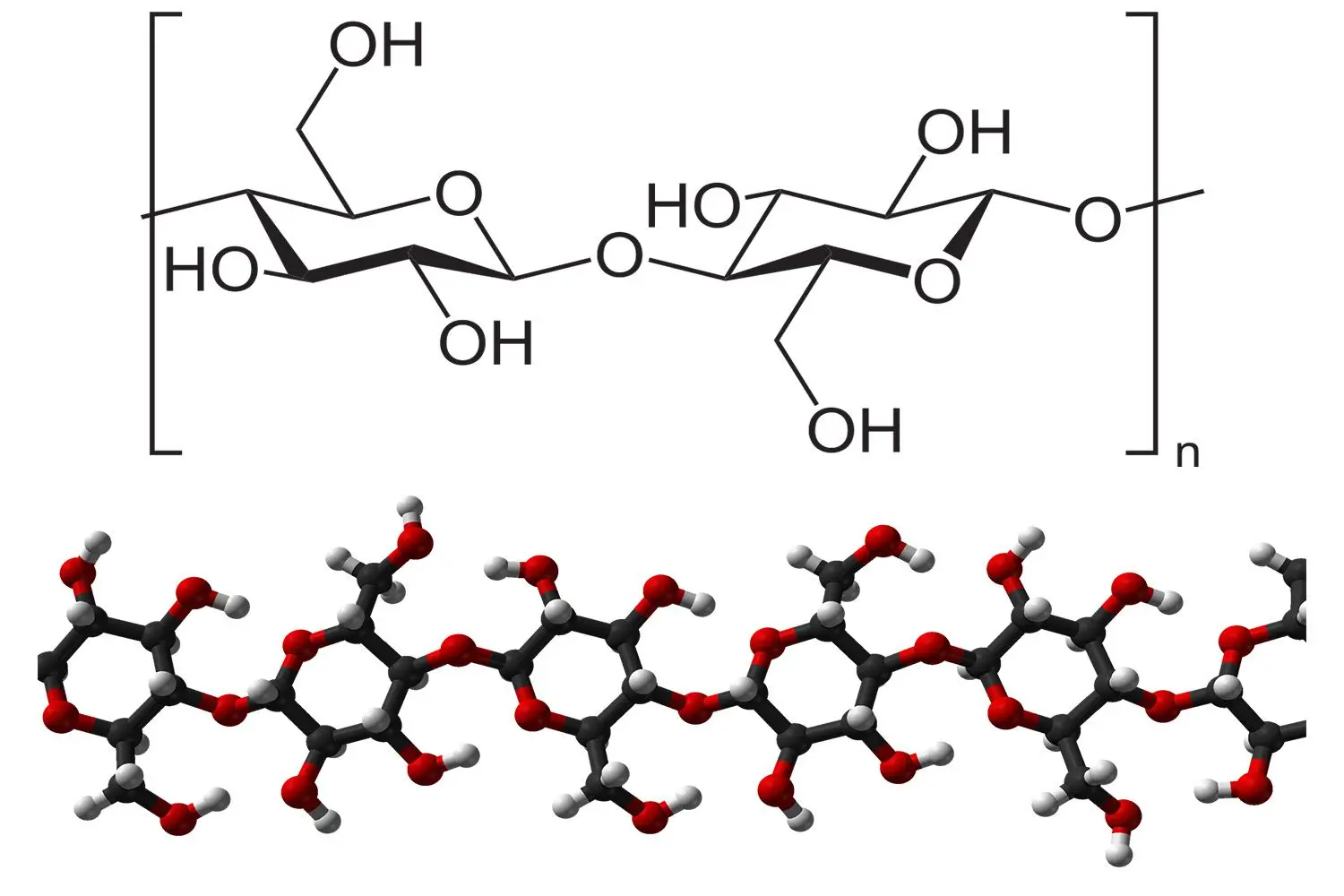
گلیکوژن، یک بیوپلیمر شاخهای متشکل از زنجیرههای خطی گلوکز است. طول متوسط هر زنجیره حدود 8 تا 12 واحد گلوکز و 200۰ تا 60000 گلوکز در هر مولکول گلیکوژن است. واحدهای گلوکز از طریق پیوندهای گلیکوزیدی (α (۱→۴ به صورت خطی به یکدیگر متصل میشوند. شاخهها از طریق پیوندهای گلیکوزیدی (α (۱→۶ بین اولین گلوکز شاخه جدید و گلوکز روی زنجیره اصلی، به آن متصل میشوند. با توجه به روش سنتز این ماکرومولکول، هر گرانول آن در هسته خود یک پروتئین گلیکوژنین دارد.
ساختار :
زنجیره های خطی ۸ تا ۱۲ واحدی گلوکز، اجزای تشکیل دهنده گلیکوژن بوده و در مجموع تعداد کل گلوکزها در یکی از این مولکول های پلی ساکاریدی، ۲۰۰۰ تا ۶۰۰۰۰ می باشد. پیوندهای گلیکوزیدی α ۱و۴، اتصال دهنده واحدهای گلوکز به شکل خطی و پیوندهای گلیکوزیدی α ۱و۶، اتصال دهنده شاخه ها در این ماکرومولکول می باشند.
عملکرد
۱. عملکرد ذخایر گلیکوژن کبدی
بدن معمولا از ذخیره گیلیکوژن کبد برای بهبود تنظیم مقدار گلوکز (قند) خون استفاده میکند. بدن قند خون را بهدقت با هورمونهای گلوکاگون و انسولین تنظیم میکند. وقتی گلوکز خون خیلی کم میشود (هیپوگلیسمی)، پانکراس گلوکاگون بیشتری ترشح میکند. گلوکاگون گلیکوژن ذخیره در کبد را تحریک میکند تا دوباره به گلوکز تبدیل شود و بتواند وارد جریان خون شود. این فرایند گلیکوژنولیز نامیده میشود. وقتی گلوکز در خون جریان داشته باشد، سلولهای سراسر بدن میتوانند از آن برای تأمین انرژی خود استفاده کنند.
علاوهبر این، ذخایر گلیکوژن کبدی تا حدی در عملکرد عضلات حین ورزشکردن نقش دارد. در شروع ورزش، کبد شروع به تجزیه گلیکوژن میکند تا مقدار گلوکز خون را حفظ کند، چون عضلات فعال بدن مدام از گلوکز خون برای تأمین انرژی استفاده میکنند. بااینحال عضلات برای بهبود عملکرد حین فعالیت بدنی، اول از ذخایر گلیکوژن خود استفاده میکنند.

۲. عملکرد ذخایر گلیکوژن عضلانی
گلیکوژن عضلانی معمولا نقش منبع سوخت متابولیک برای عضلات را ایفا میکند. برای اینکه بتوانید حرکت کنید، عضلات بدنتان به انرژی زیادی نیاز دارند. اگر عضلات شما برای دریافت این انرژی به گلوکز موجود در جریان خون متکی باشند، گلوکز خون بهسرعت افت میکند. به همین دلیل بدن سهچهارم کل گلیکوژن را در ماهیچههای اسکلتی ذخیره میکند. به این ترتیب عضلات بدن منبع انرژی ثابتی دارند (بهخصوص در حین ورزش)، بدون اینکه تأثیر چشمگیری بر میزان گلوکز خون شما داشته باشند.
سرعت کاهش گلیکوژن عضلانی به شدت فعالیت بدنی بستگی دارد؛ هرچه شدت تمرین بیشتر باشد، سرعت تمامشدن ذخیره گلیکوژن عضلانی بیشتر میشود. بنابراین فعالیت شدید مانند دویدن مکرر ممکن است بهسرعت ذخایر گلیکوژن سلولهای عضلانی فعال را کاهش دهد، حتی اگر کل زمان فعالیت نسبتا کوتاه باشد. هنگامی که کربوهیدرات کافی مصرف میکنید، ذخیره گلیکوژن عضلانی مجددا شارژ میشود.
بیماری GSD چیست ؟
بیماری ذخیره گیلیکوژن (GSD) نوعی بیماری ارثی نادر است که بهسبب آن فرد بدون آنزیمهایی متولد میشود که برای ساخت یا تجزیه گلیکوژن ضروریاند. از آنجایی که بدن از آنزیمهای مختلفی برای پردازش گیلیکوژن استفاده میکند، بیماری ذخیره گلیکوژن نیز انواع مختلفی دارد. این عارضه بیشتر اوقات منجر به آسیب کبدی و ضعف عضلانی میشود. در بسیاری از انواع این بیماری، علائم اولیه در نوزادان یا کودکان بروز میکنند.

مقدار گلیکوژن بدن با چه آزمایشهایی مشخص میشود ؟
هیچ آزمایش خاصی وجود ندارد که فقط مقدار گلیکوژن را اندازهگیری کند. میزان گلیکوژن بدن شما بر اساس مقدار فعالیت و کربوهیدراتی که در طول روز میخورید، مدام در نوسان است. آزمایشهای معمولی که پزشکان برای بررسی وضعیت ساخت و تجزیه گلیکوژن بدن و تشخیص بیماری ذخیرهسازی گلیکوژن تجویز میکنند، عبارتاند از:
- آزمایش خون: بررسی مقدار گلوکز موجود در خون نشان میدهد که بدن بهدرستی از گلیکوژن استفاده میکند یا خیر. افراد مبتلا به بیماری ذخیرهسازی گلیکوژن معمولا قند خون کمی دارند.
- سونوگرافی شکم: پزشک بهکمک این آزمایش تصویربرداری میتواند ببیند کبد بزرگ شده است یا خیر.
- بیوپسی بافتی: ممکن است پزشک گرفتن نمونهای از بافت عضله یا کبد را برای اندازهگیری مقدار گلیکوژن یا آنزیمهای موجود تجویز کند.
- تست ژنتیک: گاهی پزشک با تجویز آزمایش ژنتیک بررسی میکند که فرد حامل ژن بیماری ذخیره گلیکوژن هست یا خیر.
متابولیسم
متابولیسم به معنای سوخت و ساز است. گلیکوژن، در بدن طی فرایندی به نام گلیکونئوژنز ساخته و طی فرایندی به نام گلیکوژنولیز تجزیه میشود. در ادامه این دو مکانیسم توضیح داده شدهاند.
سنتز گلیکوژن
سنتز گلیکوژن، برخلاف تجزیه، درونزا است یعنی برای انجام شدن به ورودی انرژی نیاز دارد. انرژی برای سنتز گلیکوژن از یوریدین تری فسفات (UTP) تأمین میشود که در واکنش کاتالیز شده توسط UTP – گلوکز- 1- فسفات یوریلیل ترانسفراز با گلوکز- 1- فسفات واکنش داده و UDP- گلوکز را تشکیل میدهد. گلیکوژن، از مونومرهای UDP- گلوکز در ابتدا توسط پروتئین گلیکوژنین که دارای دو لنگر تیروزین برای کاهش انتهای گلیکوژن است، سنتز میشود زیرا گلیکوژنین یک همودیمر (تشکیل شده از دو واحد یکسان) است.
پس از افزودن حدود هشت مولکول گلوکز به یک باقیمانده تیروزین، آنزیم گیلیکوژن سنتاز به تدریج با استفاده از UDP- گلوکز، به انتهای احیای زنجیره گلیکوژن، با پیوند (α (۱→۴، گلوکز اضافه زنجیره گلیکوژن را طویل میکند.
آنزیم منشعب کننده گلیکوژن، انتقال قطعهای از شش یا هفت باقیمانده گلوکز را به انتهای غیر احیای گلیکوژن و روی گروه هیدروکسیل متصل به کربن شماره ۶، کاتالیز میکند. آنزیم شاخه ساز میتواند فقط بر روی شاخهای که حداقل 11 باقی مانده دارد عمل کند و آنزیم ممکن است برای ادامه کار خود، به همان زنجیره گلوکز یا زنجیرههای گلوکز مجاور منتقل شود.
تجزیه گلیکوژن
گلیکوژن، توسط آنزیم گلیکوژن فسفریلاز از انتهای غیر احیای زنجیره، شکافته میشود و مونومرهای گلوکز – 1- فسفات تولید میکند:
در داخل بدن، فسفرولیز در جهت تجزیه گیلیکوژن پیش میرود چون به طور معمول، نسبت فسفات و گلوکز- 1- فسفات بیشتر از 100 است. سپس گلوکز- ۱- فسفات توسط آنزیم فسفو گلوکوموتاز به گلوکز 6 فسفات (G6P) تبدیل میشود. برای از بین بردن شاخههای (α (۱→۶ در گلیکوژنِ منشعب و تغییر شکل زنجیره به یک پلیمر خطی، یک آنزیم ویژه لازم است. مونومرهای G6P تولید شده دارای سه سرنوشت احتمالی هستند:
- G6P میتواند در مسیر گلیکولیز ادامه یابد و به عنوان سوخت استفاده شود.
- G6P میتواند از طریق آنزیم گلوکز-6-فسفات دهیدروژناز به مسیر پنتوز فسفات وارد شود و NADPH و 5 قند کربن تولید کند.
- در کبد و کلیه، G6P میتواند توسط آنزیم گلوکز 6- فسفاتاز دی فسفریله و دوباره به گلوکز تبدیل شود. این آخرین مرحله در مسیر گلوکونئوژنز است.
ترشح گلیکوژن
گلیکوژن در شرایط مختلفی با تولید هورمون گلوکاگون، توسط کبد آزاد میشود از جمله:
- در پاسخ به موقعیتهای استرس زا
- هنگام بیدار شدن (این روند به عنوان پدیده سپیده دم شناخته میشود)
- در پاسخ به پایین بودن قند خون
- برای کمک به هضم غذا
اختلال در متابولیسم گلیکوژن
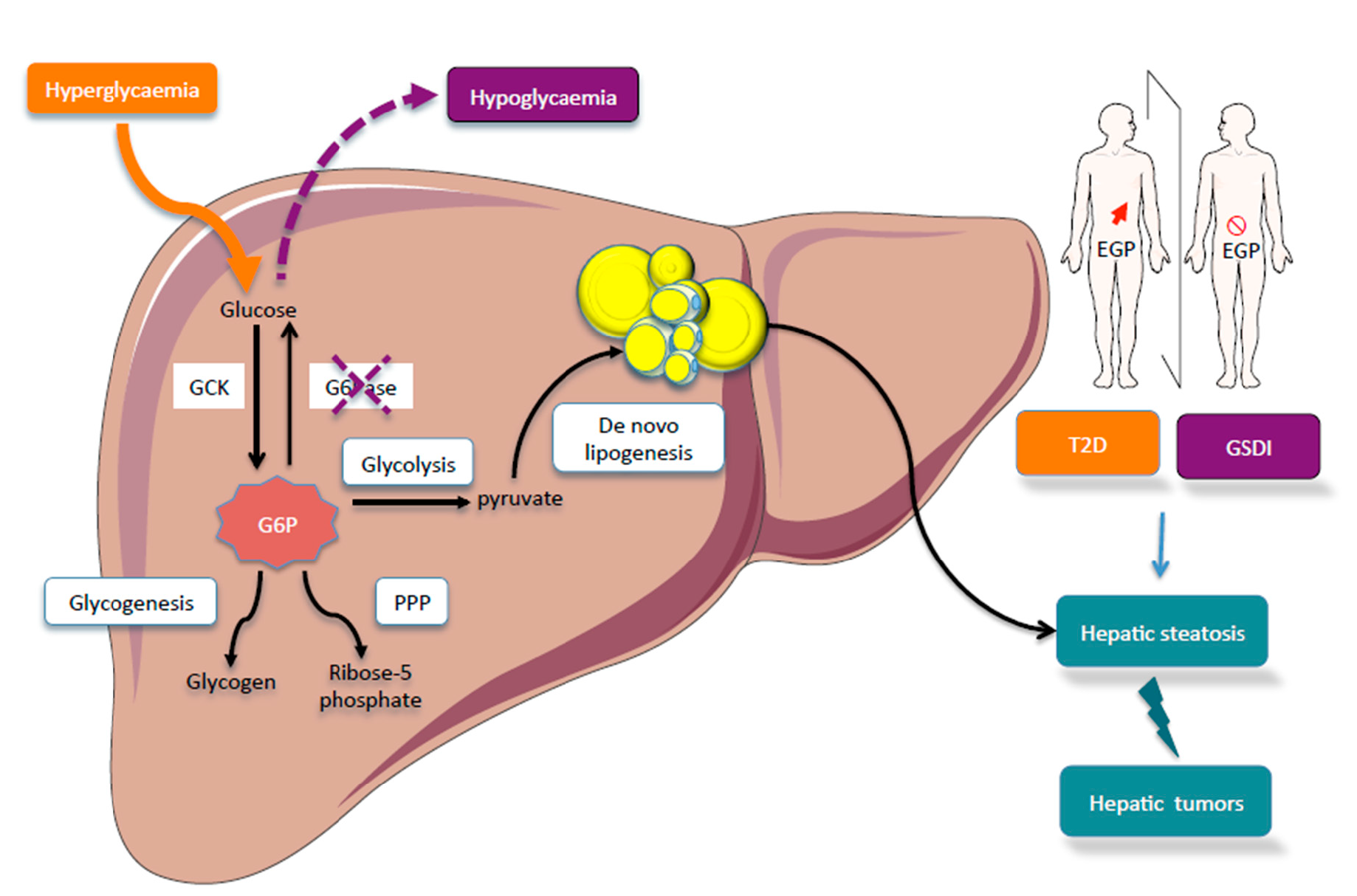
بیماریهای ذخیره گلیکوژن (GSD، همچنین گلیکوژنوز و دکسترینوز) نوعی اختلال متابولیکی هستند که به دلیل کمبود آنزیم در سنتز گیلیکوژن، تجزیه گلیکوژن یا گلیکولیز (تجزیه گلوکز) ایجاد میشوند و به طور معمول بر ماهیچهها و یا سلولهای کبدی تأثیر میگذارند. GSD دو علت ژنتیکی و اکتسابی دارد. GSD ژنتیکی در اثر هر نوع اختلال ذاتییا ارثی در متابولیسم (آنزیمهای معیوب ژنتیکی) درگیر در این فرآیندها ایجاد میشود. GSD اکتسابی ناشی از مسمومیت با آلکالوئید کتانوسپرمین است.
شایعترین بیماری که متابولیسم گیلیکوژن، در آن غیرطبیعی میشود، دیابت است که در آن، به دلیل مقادیر غیر طبیعی انسولین، گلیکوژنِ کبد میتواند به طور غیر طبیعی تجمع یا تخلیه شود. ترمیم متابولیسم گلوکز طبیعی به طور معمول متابولیسم گلیکوژن را نیز عادی میکند. در هیپوگلیسمی (افت قند خون) ناشی از ترشح زیاد انسولین، سطح گلیکوژنِ کبد زیاد است اما سطح بالای انسولین مانع از گلیکوژنولیز لازم برای حفظ سطح طبیعی قند خون میشود.
تقریباً ۲ الی ۳ کودک در هر صد هزار تولد (1 در ۴۳ هزار) به نوعی از بیماریهای ذخیره گلیکوژن مبتلا هستند. در ایالات متحده تخمین زده میشود که این موارد یک مورد در هر ۲۰ هزار تا ۲۵ هزار تولد باشد. میزان بروز این بیماری در هلند، 1 در هر ۴۰ هزار تولد است. شیوع اختلال در متابولیسم گلیکوژن در مکزیک حدود ۶ مورد از هر هزار نوزاد پسر را نشان میدهد.
بیماری پمپ
«بیماری پمپ» (Pompe Disease) در اثر جهش در ژن GAA ایجاد میشود که اسید لیزوزومی α- گلوکوزیداز را کد میکند که اسید مالتاز نیز نامیده میشود و بر عضلات اسکلتی و قلبی تأثیر میگذارد. اسید مالتاز در تجزیه گلیکوژن نقش دارد و جهشهای ایجاد کننده این بیماری، منجر به تجمع مضر گلیکوژن در سلول میشوند. بیماری پمپ نوعی اختلال ژنتیکی نادر و ارثی است که باعث ضعف عضلانی خواهد شد، پیشرونده است، با گذشت زمان بدتر و در موارد شدید باعث مرگ میشود.
سه نوع بیماری پمپ وجود دارند که به ترتیب نام برده شدیدتر میشوند:
- فرم بزرگسالان
- فرم جوانی
- فرم کودکی
نوع کودک در صورت عدم درمان منجر به مرگ در سن یک تا دو سالگی خواهد شد.
بیماری مک آردل
دو ایزوفرم گلیکوژن فسفریلاز وجود دارند که توسط دو ژن جداگانه رمزگذاری شدهاند. کمبود در ایزوفرم عضله یا میوفسفریلاز (رمزگذاری شده توسط PYGM) منجر به اختلال در گلیکوژنولیز و GSD نوع V، به نام «بیماری مک آردل» (McArdle Disease) میشود. علائم اغلب در کودکان قابل تشخیص هستند، اما بیماری ممکن است تا بزرگسالی تشخیص داده نشود. علائم شامل درد و ضعف عضلانی، میوگلوبینوریا و گرفتگی عضلات هستند و درصد کمتری از بیماران ممکن است مشکلات قلبی عروقی را نشان دهند.
این بیماری میتواند کشنده باشد. اکثر بیماران سطح بالایی از کراتین کینز را در خون نشان میدهند. روش ترجیحی تشخیص GSD نوع V، تجزیه و تحلیل ژنتیکی است. هیچ درمانی برای این بیماری وجود ندارد اما یک مطالعه نشان داده است که مصرف ساکارز قبل از ورزش میتواند ظرفیت عضلات را افزایش دهد و ورزش هوازی متوسط نیز به بهبود عملکرد عضلات و افزایش عمر بیماران کمک میکند.
بیماری هرس
کمبود گلیکوژن فسفریلاز کبدی یا بیماری GSD نوع VI، در اثر کمبود فعالیت ایزوفرم کبدی گلیکوژن فسفوریلاز (رمزگذاری شده توسط PYGL) ایجاد میشود. «بیماری هرس» (Hers’ Disease) همچنین شامل افرادی با جهش در ژنهای دیگری است که بر عملکرد PYGL تأثیر میگذارند. علائم این بیماران در مقایسه با GSD نوع V بسیار متفاوت هستند. بیماران مبتلا به GSD نوع VI، سطح کراتین کیناز و اسید اوریک طبیعی دارند. این بیماری اغلب از اوایل کودکی شروع میشود و به طور قابل توجهی خوشخیم است.
مبتلایان به طور معمول با تاخیر رشد و هپاتومگالی روبرو میشوند. از آنجا که گلیکوژنولیز کبد مختل شده است، افت قند خون کتوتیک و همچنین چربی خون شایع هستند. اغلب این شرایط با افزایش سن بهبود مییابند و درمان غیر ضروری است. افرادی با GSD نوع IX فنوتیپ بسیار مشابهی با GSD نوع VI از خود نشان میدهند. GSD نوع IX به دلیل کمبود ایزوفرم کبدی گیلیکوژن فسفوریلاز ایجاد میشود.

بیماری آندرسن
«بیماری آندرسن» (Andersen Disease) یا GSD نوع چهارم، در اثر جهش در ژن GBE1 ایجاد میشود که آنزیم منشعبکننده گلیکوژن را کد میکند و بر روی عضلات و کبد تأثیر میگذارد. علائم می توانند از همان اوایل جنینی (هیدروپس داخل رحمی) شروع شوند و به دلیل هیپوتونی و کاردیومیوپاتی شدید، مرگ پریناتال رخ دهد. در غیر این صورت علائم در چند ماهگی بروز میکنند و نارسایی در رشد، هپاتوسپلنومگالی و سیروز کبدی پیشرونده معمولا منجر به مرگ بیمار تا 5 سالگی خواهند شد.
عوارض ناشی از این بیماری میتوانند کشنده باشند. کاهش قند خون ناشتا معمول نیست مگر اینکه سیروز کبدی قابل توجهی وجود داشته باشد. در بزرگسالان، GSD نوع IV خفیفتر است و میتواند به صورت میوپاتی جدا یا به عنوان یک اختلال چند سیستمی ظاهر شود. این افراد علائمی از درگیری نورون حرکتی فوقانی و تحتانی را نشان میدهند که عوارضی همچون بیاختیاری ادرار و اختلال در راه رفتن و خوابرفتگی یا «پارستزی» (Paresthesia) اندامهای تحتانی را به دنبال دارد.
در مبتلایانی که معمولاً بیش از 30 سال دارند، به دلیل کاهش فعالیت GBE1، بیماری آندرسن ممکن است با بیماری پلی گلوئوزان که بر سیستم عصبی مرکزی و محیطی تأثیر میگذارد، اشتباه گرفته شوند. تشخیص GSD نوع IV نیاز به نمونهبرداری از گلیکوژن غیرطبیعی و رنگآمیزی بافتی و تجزیه و تحلیل نمونه با میکروسکوپ الکترونی دارد. عدم فعالیت آنزیم شاخهساز در کبد، عضله، فیبروبلاست، لکوسیت یا گلبولهای قرمز، بیماری را تأیید میکنند. وجود جهش ژنتیکی و تجزیه و تحلیل ژنومی نیز قابل انجام است.
هیچ درمانی برای GSD نوع IV وجود ندارد و مراقبتهای پزشکی بر حفظ نوروموگلایسمی متمرکز هستند. تغذیه مناسب میتواند به بهبود عملکرد کبد و عضله کمک کند و همچنین نتایج طولانی مدت را برای این بیماران به همراه داشته باشد. برای کسانی که بیماری کبدی دارند، ممکن است پیوند کبد ضرورت یابد.
بیماری لافورا
اختلالات متابولیسم گلیکوژن همیشه با اختلال عملکرد کبد یا عضله ارتباط داشتند زیرا اکثر ذخایر گلیکوژن در بدن انسان در این بافتها یافت میشوند. با این حال، در اکثر سلولها مقادیر قابل توجهی گیلیکوژن وجود دارد و برخی از مطالعات اخیر بر اهمیت گلیکوژن در مغز متمرکز شدهاند. بیماری «لافورا» (Lafora)، نوعی از بیماری ژنتیکی اتوزومال مغلوبِ صرع است. شاخصه اصلی این بیماری، وجود اجسام انسدادی (اجسام لافورا) در اکثر اندامها از جمله مغز است.
اجسام لافورا فرم غیر طبیعی گلیکوژن هستند که به عنوان سوخت قابل تجزیه نیستند. این اجسام، حاوی مقادیر زیادی پلی گلوکوزان هستند که تجمع آنها باعث آسیب و مرگ سلولها میشود. تجمع این اجسام در مغز عامل اکثر علائم مانند تشنج، آتاکسی، میوکلونوس و پیشرفت تدریجی زوال عقل شدید است. بیماران معمولاً تا 30 سالگی میمیرند و در حال حاضر درمانی برای آن وجود ندارد. لافورا حدود 10 برابر بیشتر از گلیکوژن، حاوی فسفات است. در غیاب لافورین، گلیکوژن بیش از حد فسفریله و باعث شکلگیری اجسام لافورا میشود.
درمان بیماری GSD
درمان به نوع بیماری ذخیره گلیکوژن بستگی دارد. GSD I به طور معمول با وعدههای غذایی كوچک حاوی كربوهیدرات و نشاسته ذرت، تحت عنوان درمان نشاسته ذرت اصلاح شده، برای جلوگیری از افت قند خون درمان میشود. در حالی كه سایر درمانها، ممكن است شامل آلوپورینول و عامل تحریک كلنی گرانولوسیت انسانی باشند. استفاده از گلوکاگون نیز یک روش درمانی متداول برای این نوع کاهش قند خون است.
رژیم غذایی
میزان و کیفیت تغذیه و همچنین تحرک، بر تولید یا سوخت گلیکوژن تأثیر دارند. در رژیمهای کم کربوهیدرات مانند اتکینز یا رژیم کتوژنیک، که در آنها منابع اصلی سنتز گلوکز (کربوهیدرات) به طور ناگهانی محدود میشوند، ذخایر گلیکوژنِ بدن میتوانند به شدت تخلیه شوند و در نهایت علائمی مانند خستگی و گیجی یا به اصطلاح آنفولانزای کتویی به وجود میآیند. پس از عادت بدن به رژیم غذایی جدید و تنظیم تولید هورمونها و قند خون، بدن دوباره شروع به تجدید ذخایر گلیکوژنِ خود میکند و علائم کاهش مییابند.
کاهش وزن هم میتواند همین تأثیرات را در ذخیره گلیکوژن داشته باشد. در ابتدا ممکن است کاهش وزن سریع باشد، بعد از یک دوره زمانی، وزن ثابت بماند یا حتی بیشتر شود. این پدیده تا حدودی به دلیل ترکیب گلیکوژن با آب است. آب موجود در این مولکول سه تا چهار برابر وزن خود گلوکز است. به همین دلیل، وزن در ابتدای رژیم، به علت کاهش آب، به سرعت کم میشود. با گذشت زمان، ذخایر گلیکوژن تجدید خواهند شد و آب از دست رفته شروع به بازگشت میکند. وقتی این اتفاق افتاد، کاهش وزن ممکن است متوقف یا ثابت شود.
چه غذاهایی گلیکوژن دارند ؟
سلولهای عصبی و نورونها، برای فعالیت صحیح خود به مقدار کافی گلوکز نیاز دارند. بدن بلافاصله از گلوکز مورد نیاز خود استفاده میکند و بقیه را به عنوان گلیکوژن در کبد و عضلات ذخیره میکند که هنگام پایین بودن قند از این ذخایر جهت عملکرد صحیح ارگانهای مختلف خصوصا مغز استفاده میشود. از آنجا که گلیکوژن منبع سوخت بدن است، خوردن برخی مواد غذایی برای وجود سطح کافی از گلیکوژن ضرورت دارد.
- میوهها: میوههای تازه پر از کربوهیدراتهای ساده به شکل قند میوه یا فروکتوز هستند. این نوع کربوهیدراتها در روده کوچک به سرعت و در یک مرحله هضم میشوند و ذخایر گلیکوژن را تقویت میکنند.
- سبزیجات نشاستهدار: نشاسته نوعی کربوهیدرات پیچیده است که تجزیه آن در دهان آغاز و در نهایت به صورت گلوکز جذب میشود. بزاق دهان، مولکولهای نشاسته پیچیده را به مالتوز تبدیل میکند که یک کربوهیدرات ساده است. هنگامی که مالتوز به روده کوچک میرسد، به گلوکز تبدیل و وارد جریان خون میشود. برخی صیفیجات مانند سیب زمینی، کدو و سیبزمینی شیرین، غنی از نشاسته هستند. دستگاه گوارش نشاسته مورد نیاز را به سرعت به قند تبدیل و به عنوان گلیکوژن ذخیره میکند.
- غذاهای سبوس دار: یک برش نان گندم کامل، یک سوم فنجان ماکارونی با آرد گندم یا یک سوم فنجان برنج قهوهای، هر کدام 15 گرم کربوهیدرات دارند که ترکیبی از قندهای ساده و نشاسته است. انتخاب غلات کامل به جای انواع سفید یا فرآوری شده، دریافت فیبر کافی در کنار کربوهیدرات را تضمین میکند که اهمیت فراوانی دارد چون برای هضم و تبدیل کربوهیدرات به قند ساده و ورود گلوکز به خون و ساخت گلیکوژن، ضروری است.

گلیکوژن در ورزش
اکثر ورزشکاران در هر دقیقه دو تا سه گرم کربوهیدرات میسوزانند. حتی در ورزش با شدت کم، در هر دقیقه یک تا دو گرم کربوهیدرات متابولیزه میشود که البته این میزان با تمرین قابل تنظیم است. ورزشکاران در صورت سوخت کامل 300 تا 500 گرم گلیکوژن در خود ذخیره میکنند و این با حدود 90 تا 120 دقیقه ورزش شدید برابر است. گلیکوژن به سرعت میسوزد اما ذخایر آن به کندی و معمولاً با سرعت دو تا پنج درصد در ساعت، پس از ورزش دوباره پر می شوند. بازیابی ذخایر خالی گلیکوژن ممکن است یک روز یا بیشتر طول بکشد. به سه دلیل، گلیکوژن برای ورزشکاران استقامتی اهمیت دارد:
- منبع اصلی سوخت: در تمرینات و مسابقات پیشرفته، برای انجام حداکثر توانایی باید از گلیکوژن استفاده کرد. ذخیره کم گلیکوژن در ورزشکاران میتواند باعث خستگی و حتی پروتئینسوزی و کاهش عضلات شود. این یکی از دلایلی است که دسترسی کم به گلیکوژن، به مرور زمان باعث کاهش عملکرد و حتی سندرم تمرین بیش از حد میشود.
- بهبود آسیبهای عضلانی: گلیکوژن به عضلات کمک میکند تا ترمیم شوند و پس از ورزشی با شدت زیاد، از سوخت و ساز پروتئین عضله برای تأمین انرژی جلوگیری میکند. با پر کردن مجدد ذخایر گلیکوژن میتوان عضلات را حفظ و بهبودی را تسریع کرد. افزایش منابع گلیکوژن به آمادگی سریعتر بدن و عضلات هم کمک میکند.
- بهبود انجام تمرینات در حالت تخلیه گلیکوژن: تمرین در حالت تخلیه گلیکوژن میتواند کارایی انجام تمرینات هوازی را بهبود دهد. در حالی که بدن به طور کلی برای عملکرد در سطح بالا به گلیکوژن نیاز دارد اما میتوان برای استفاده استراتژیک از ذخایر گلیکوژن آموزش دید. دویدن در حالت تخلیه ذخایر گلیکوژن، میتواند مارکرها را برای سازگاری با تمرینات تقویت کرده و چربیسوزی را افزایش دهد.
برخی از ورزشکاران برای افزایش این اثر، از رژیم کم چربی (LCHF) و کم کربوهیدرات استفاده میکنند تا چربیها با سرعت به نسبت بالایی بسوزند. با این حال، رژیمهای غذایی LCHF پیچیده و بحث برانگیز هستند و باید فقط برای اهداف آموزشی و هنگام آمادگی برای مسابقات، با شدت کم و زیر نظر یک متخصص انجام شوند.

تخلیه و پایداری هنگام ورزش
ورزشکاران مسافتهای طولانی مانند دو و میدانی ماراتن، اسکی بازان و دوچرخه سواران به طور معمول دچار کاهش گلیکوژن میشوند، وقتی تقریباً تمام ذخایر گلیکوژنِ ورزشکار پس از مدتها ورزش و بدون مصرف کربوهیدرات کافی تخلیه شود، این پدیده اصطلاحا «برخورد به دیوار» نام دارد. برای جلوگیری از این پدیده، با سه روش از تخلیه گلیکوژن، جلوگیری میشود:
- حین ورزش، کربوهیدراتهایی با بالاترین میزان ممکن تبدیل به گلوکز خون (شاخص گلیسمی بالا) به طور مداوم بلعیده میشوند. بهترین نتیجه ممکن در این استراتژی، جایگزین کردن حدود 35 درصد از گلوکز مصرف شده، در ضربان قلب بالاتر از حدود 80 درصد از حداکثر ضربان است.
- از طریق تمرین استقامتی و رژیمهای تخصصی (به عنوان مثال روزهداری، تمرین استقامتی با شدت کم)، بدن میتواند فیبرهای عضلانی نوع I را برای بهبود بهرهوری در مصرف سوخت و همچنین ظرفیت کاری برای افزایش درصد اسیدهای چرب مورد استفاده به عنوان سوخت، بهبود ببخشد تا در مصرف کربوهیدرات از همه منابع موجود، صرفهجویی شود و در صورت تخلیه کربوهیدرات بدن سوخت خود را به سرعت از چربی تأمین کند.
- با مصرف مقادیر زیادی کربوهیدرات پس از تخلیه ذخایر گلیکوژن، در نتیجه ورزش یا رژیم غذایی، بدن میتواند ظرفیت ذخیرهسازی ذخایر گلیکوژنِ داخل عضلانی را افزایش دهد. این فرآیند به عنوان بارگذاری کربوهیدرات شناخته میشود. به طور کلی، شاخص گلیسمی منبع کربوهیدرات مهم نیست زیرا حساسیت به انسولین عضلانی در نتیجه کاهش موقتی گلیکوژن، افزایش مییابد.
هنگام کمبود گلیکوژن، ورزشکاران اغلب خستگی مفرط را تا حدی تجربه میکنند که بهبود آن دشوار است. بهترین دوچرخه سواران حرفهای جهان به طور معمول یک مسابقه 4 تا 5 ساعته را درست در حد کاهش گلیکوژن، با استفاده از سه استراتژی اول به پایان میرسانند. اگر ورزشکاران هر دو کربوهیدرات و کافئین را به دنبال ورزشهای قدرتی مصرف کنند، ذخایر گلیکوژنِ آنها با سرعت بیشتری تجدید میشود.